首頁故事
清華用晶體結構解開腦部鈣化之謎 治療失智露曙光【2020.08.31秘書處】
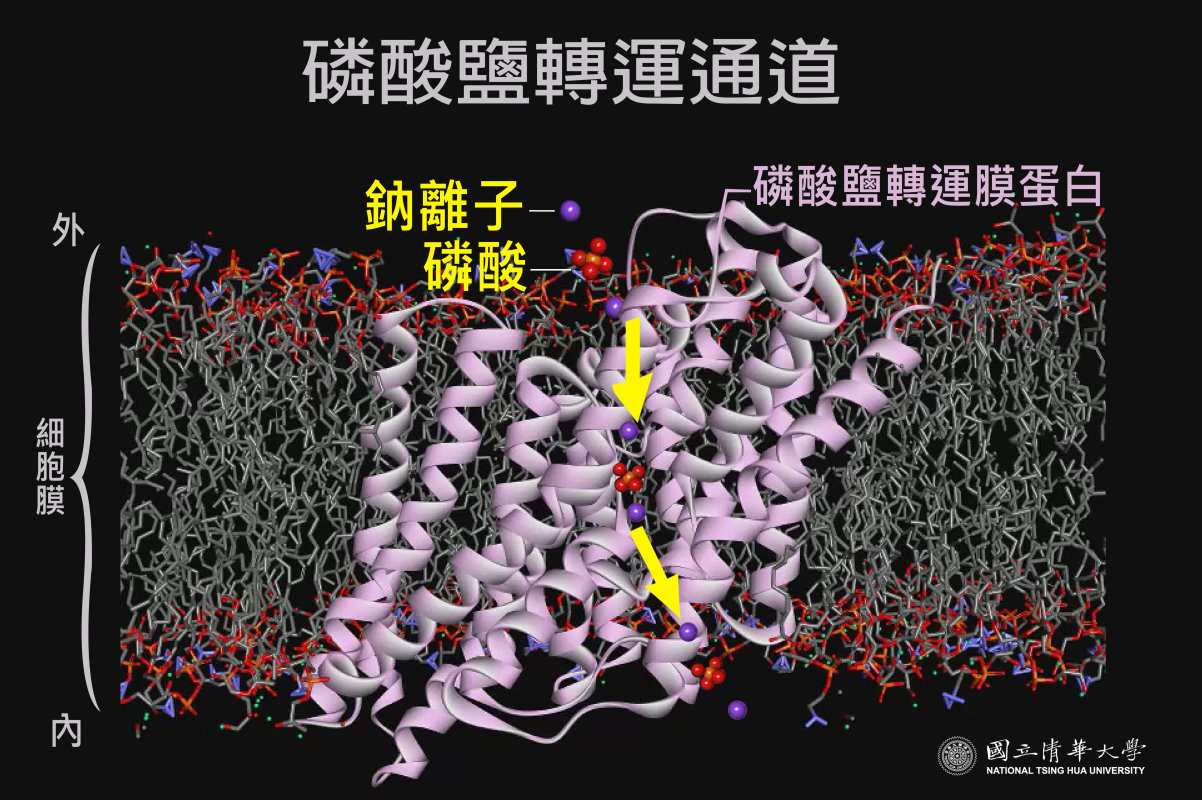
類帕金森氏症、阿茲海默症等神經退化病症起因之一是腦部基底核出現鈣化,腦細胞表面的膜蛋白通道阻塞,無法傳送信號分子及營養到細胞內。本校生物資訊與結構生物研究所孫玉珠教授研究團隊,最近與中央研究院分子生物所蕭傳鐙研究員實驗室合作,創全球之先,解開了「磷酸鹽轉運膜蛋白」分子結構之謎,使失智症的治療露出一線曙光。
這項由科技部尖端計劃支持的研究成果登上了今年8月的國際頂尖期刊《科學前緣》(Science Advances),成為台灣膜蛋白研究領域的重要里程碑。
孫玉珠教授表示,膜蛋白是鑲嵌在細胞膜上的蛋白質,負責傳遞信號並供應能量到細胞內,因此在藥物開發上扮演非常重要的角色。磷酸鹽轉運膜蛋白則是將磷酸鹽及鈉離子運送到腦細胞內的重要通道,一旦發生病變,通道阻塞,磷酸鈣就會沈澱在細胞膜表面,最終導致腦部基底核鈣化,產生類帕金森氏症的動作障礙或阿茲海默症等神經退化性病變。
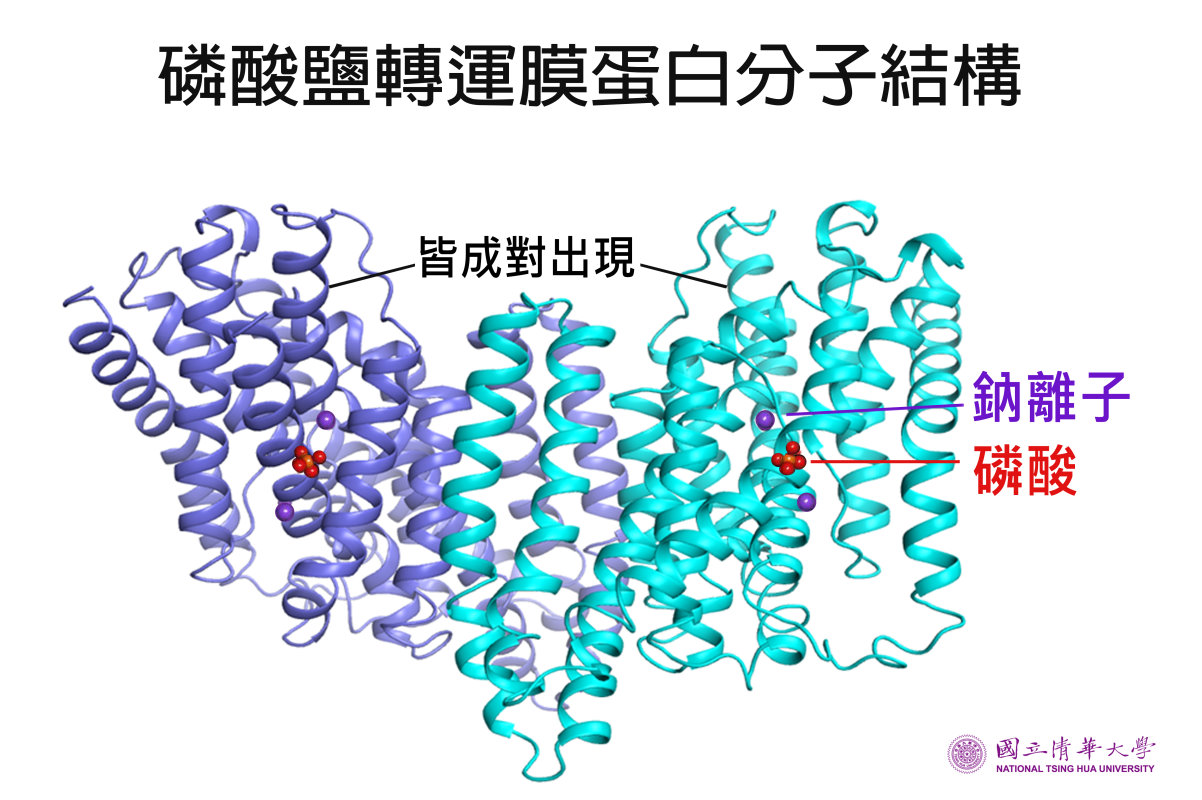
孫玉珠教授領導的研究團隊利用國家同步輻射中心的光源,進行X光繞射磷酸鹽轉運膜蛋白晶體,得出繞射圖後進行運算,成功解析出膜蛋白的立體結構,並透過基因序列找到膜蛋白突變的確切位置,讓人類得以首次「看到」失智症的病因。
孫玉珠教授指出,解析磷酸鹽轉運膜蛋白並找到突變位置,已為治療腦部鈣化踏出了第一及第二步,接下來將與醫師合作,以此結構為基礎來設計藥物,利用電腦計算及模擬,實驗篩選出有效的化學小分子,讓膜蛋白恢復正常,「重新打通阻塞的傳遞通道,撥開失智症患者腦中的迷霧。」
中研院分子生物研究所蕭傳鐙研究員是生物物理專家,也在這項創新研究中扮演關鍵角色。在孫玉珠教授研究團隊解析出磷酸鹽轉運膜蛋白的立體結構後,蕭傳鐙研究員利用人工細胞膜,驗證目標位置發生突變是否令膜蛋白喪失運送磷酸鹽的功能。
人體有3到4萬種蛋白質,膜蛋白是其中最重要、也最難以研究解開的難題。但孫玉珠教授投入的正是這塊最困難的研究領域,她在8年前解析「質子泵焦磷酸水解酶」膜蛋白,成為全台第一個解析出膜蛋白分子結構的研究團隊;之後又花了5年解析磷酸鹽轉運膜蛋白分子結構。
要解析膜蛋白分子結構,首先要培養出膜蛋白晶體,才能用X光繞射的方法看到其中的結構。孫玉珠教授展示顯微鏡下只有芝麻粒十分之一大小的膜蛋白晶體,「它有稜有角、晶瑩剔透,且蘊藏著重要的分子結構資訊,對我來說比鑽石還珍貴美麗。」
主要負責培養膜蛋白晶體的是研究團隊中的本校生資所博士後研究員蔡佳吟。她說,培養第一顆的磷酸鹽轉運膜蛋白晶體就花了一年的時間,之後又耗時一年才得出優化穩定的晶體。「晶體就跟孩子一樣,需要投入耐心及細心來培養。」蔡佳吟笑說。
-
十年前,清華曾有位只能看見10公分世界的「微光女孩」莊靜潔,巡迴演講上百場,用她的生命故事激勵... (繼續閱讀)
-
本校於12月11日舉行校務發展諮詢委員會,諮詢委員們針對培養人才、發展後醫學領域、疫情後的挑戰三... (繼續閱讀)
-
本校運動員在今年的全國大專校院運動會表現亮眼,榮獲20金14銀18銅佳績,刷新校史、創下全大運得牌... (繼續閱讀)
-
本校特殊選才「拾穗計畫」今天放榜,今年有1193位學生提出申請,包括大一不分系的清華學院學士班及... (繼續閱讀)
-
為保育瀕危蕨類,本校在生命科學系特聘李家維教授的規畫下,從屏東的辜嚴倬雲植物保種中心移植烏來... (繼續閱讀)
-
許多已申請上國外一流大學及研究所的台生因疫情「卡關」,暫時無法出國。本校今年9月為這些學生設... (繼續閱讀)